



当グループは非侵襲的循環器画像診断の包括的な臨床と研究ならびに教育を行っています。
なかでも心臓核医学と心臓CT/MRIを用いた画像診断を活動の主軸としています。
心臓核医学
心臓核医学検査は虚血性心疾患患者における心筋血流,代謝,機能に関する生理学的画像を提供できることが特徴であり、主に形態あるいは解剖学的画像を提供する冠動脈造影検査や冠動脈CT検査などの他のモダリティと併せて、虚血性心疾患をはじめとした各種心疾患の診断、重症度評価、治療方針の決定や予後評価に広く用いられています。
当院では従来使用してきたアンガー型の検出器に代わる次世代の検出器である半導体検出器を採用した心臓専用SPECT装置「Discovery NM 530c」が2011年9月より導入され、感度および分解能の高い画像が得られるようになりました。半導体検出器の特性を生かし、アイソトープ減量による患者さんの医療被ばくを低減した、かつ撮像時間を短縮した新しい検査プロトコールにより日常検査を行っています。
負荷心筋血流SPECT検査データなどを用いた心疾患の診断、病態評価などに関する臨床研究の業績は、毎年、国際学会をはじめ、各種国内学会において発表され、学会誌に原著論文として掲載されています。

心臓CT/MRI
心臓CTでは多列化が進み、冠動脈の器質的狭窄を評価するだけでなく、プラークの性状、心房や肺静脈の形態、先天性心疾患などの評価について臨床で幅広く利用されております。心臓MRIでは、心機能評価、心筋性状やバイアビリティ評価において重要な役割を果たしております。
当院では、2018年4月より従来の64列CTからGE社製256列CT「Revolution CT」が導入されました。これにより検査時間の短縮、医療被ばくの軽減が可能となりました。MRIでは、シーメンス社製 MAGNETOM Skyra 3T MRIが導入されております。被ばくなく、心機能や形態、心筋の性状など、1回の検査で総合的な評価が可能です。

<常勤>
肥田 敏(准教授、医学博士、日本内科学会総合内科専門医/指導医、日本循環器学会専門医、日本心臓病学会特別正会員[FJCC])
小菅 寿徳(准教授、医学博士、日本内科学会総合内科専門医、日本循環器学会専門医)
斎藤 哲史(助教、医学博士、日本内科学会認定医、日本循環器学会専門医、日本心血管インターベンション治療学会認定医)
冨士田 康宏 (臨床研究医、日本内科学会認定医)
<非常勤>
森島 孝行 (兼任助教、医学博士、日本内科学会認定医、日本循環器学会専門医、日本核医学会専門医)
波多野 嗣久 (兼任講師、医学博士、日本内科学会認定医、日本循環器学会専門医、日本核医学会専門医)
五十嵐 祐子 (兼任講師、医学博士、日本内科学会認定医、日本循環器学会専門医)
柴 千恵 (兼任講師、医学博士、日本内科学会認定医、日本循環器学会専門医)
日本核医学会専門医教育病院
心臓核医学分野
当院では2011年9月より、従来使用してきたアンガー型の検出器に代わる次世代の検出器である半導体検出器を採用した心臓専用SPECT装置「Discovery NM 530c」(図1)が導入され、感度および分解能の高い画像が得られるようになりました。従来のアンガー型ガンマカメラでは99mTc製剤を用いた負荷心筋SPECTの場合、負荷時、安静時とも15-20分間の撮像が必要でしたが、Discovery NM 530c導入後は半導体検出器の特性を生かし、撮像時間は負荷時10分、安静時6分と短縮が可能となり、また検査で用いるアイソトープは従来と比較し、半分の使用量で検査を行い、患者さんの医療被ばくを低減した新しい検査プロトコールにより日常検査を行っています。
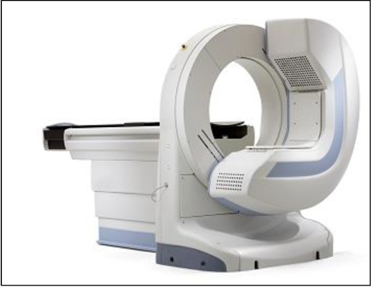
図1 心臓専用SPECT装置「Discovery NM 530c」
以下に当院で行っている心臓核医学検査を紹介します。
1)負荷心筋血流シンチグラフィ
主に心筋虚血の存在診断、心筋梗塞の診断、 予後評価・リスク層別化、 心筋バイアビリティ評価、血行再建術後の治療効果判定などの評価に用いられています。月曜日から金曜日の毎日、5-7件ずつ行っています。
心筋虚血の検出の診断精度
ACC/AHA/ASNCの心臓核医学ガイドラインでは冠動脈造影上50%狭窄以上の冠動脈疾患の診断精度は運動負荷心筋血流SPECTの感度は87%、 特異度は73%、ジピリダモール, アデノシンを用いた血管拡張薬負荷心筋血流SPECTの感度は89%、特異度は76%と高い診断精度を有しています。また201Tl と99mTc製剤の診断精度は同等であると報告されています。当院より報告した半導体検出器搭載ガンマカメラで行った負荷心筋シンチグラフィの各冠動脈ごとの有意狭窄病変(冠動脈90%狭窄またはFFR0.80以下と定義)に対する診断能を下記に示します。99mTc低投与量プロトコール(図2)と201Tlの負荷心筋シンチグラフィ(図3)
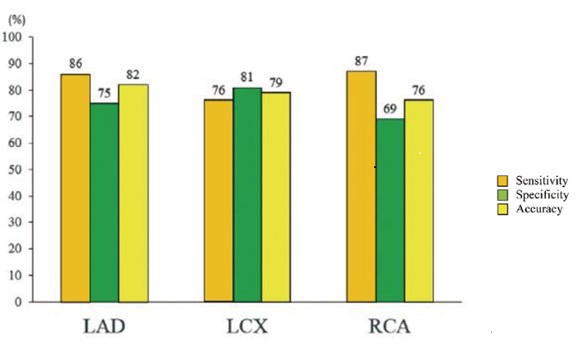
図2 99mTc低投与量負荷心筋シンチグラフィの診断精度 (Chikamori T et al. Circulation Journal 2016. 80, 1217-1224.より引用)
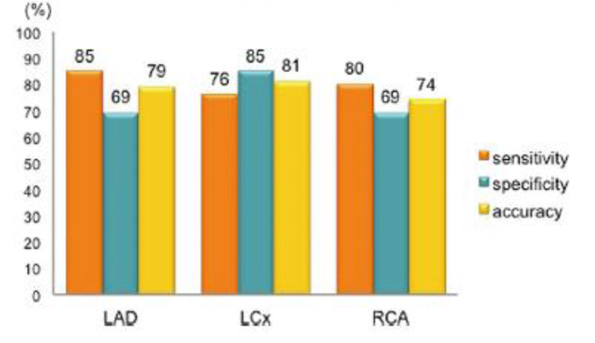
図3. 201Tl負荷心筋シンチグラフィの診断精度(Tanaka H, et al. Circulation Journal 2014; 78, 2727-2734. より引用
2018年度4月の診療報酬改定において安定狭心症に対する待機的な経皮的冠動脈インターベンション治療(PCI)に関して, 冠動脈造影上50-75%の中等度狭窄病変に対してPCIを行う場合は機能的な虚血の確認を求める算定要件が新設されました。負荷心筋血流検査は運動負荷、薬物負荷どちらも可能であり、また冠動脈CT検査が困難な慢性腎臓病や不整脈例にも対応できるため、 非侵襲的心筋虚血の診断法として今後一層, 中心的な役割を担うと考えられます。
2) 安静2核種99mTc-sestamibi/123I BMIPP シンチグラフィ
負荷をかけずに行う検査です。主に急性心筋梗塞後や不安定狭心症など急性冠症候群症例に行われています。虚血心筋では脂肪酸代謝が抑制され, 糖代謝が主なエネルギー源となります。虚血が回復してもしばらく脂肪酸代謝が抑制されているため、脂肪酸代謝イメージングである123I-β-methyl iodophenyl pentadecanoic acid (BMIPP)を用いて, 気絶心筋や冬眠心筋の評価が可能です。血流製剤である99mTc-sestamibiと脂肪酸代謝を評価する123I-BMIPPの集積の一致、不一致(乖離)を評価することにより、梗塞心筋や虚血メモリーの評価が可能です。当院では安静2核種(99mTc-sestamibi370MBq/123I BMIPP 111MBq)同時収集法にて約5.1mSVと低被ばくで行っています。
2-A) 急性心筋梗塞、不安定狭心症患者さんの評価
急性心筋梗塞患者の予後は, 主として左室駆出率, 梗塞サイズ, 残存心筋リスクに規定されます。 安静心電図同期心筋血流SPECTにより、左室駆出率と梗塞サイズの評価が可能です。 急性心筋梗塞患者において、左室全体の20%以上に及ぶ血流欠損、すなわち広範囲な心筋梗塞があると、梗塞範囲が小さい症例と比べて死亡率が高いと報告があり、梗塞範囲の評価が可能です。また急性心筋梗塞で冠動脈血行再建術を施行した患者さんの病態評価が可能です。99mTc-sestamibi/123I BMIPPシンチグラフィの集積低下が一致していれば梗塞心筋・壊死心筋であり、99mTc-sestamibi/123I BMIPPの集積に乖離があれば、その領域は冠動脈血行再建術により救済された領域と判断でき、今後同部位の左室壁運動の改善が期待できます。(図4)
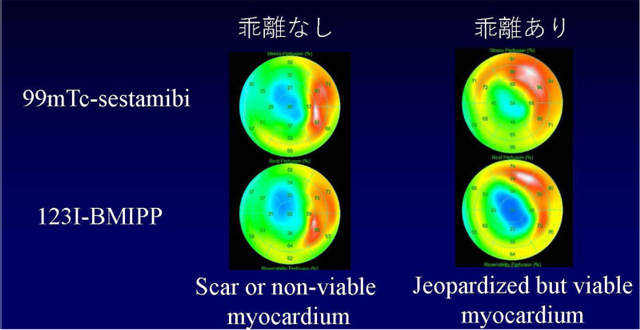
図4. 安静2核種99mTc-sestamibi/123I BMIPP シンチグラフィによる急性心筋梗塞後の評価
2)-B 123I BMIPPシンチグラフィ・123I-MIBGシンチグラフィ・その他
たこつぼ型心筋症: たこつぼ型心筋症は急性冠症候群に類似した症状、心電図変化を認め、左室心尖部の無収縮と心基部の過収縮を呈します。 しばしば急性冠症候群との鑑別が困難なことがあります。心臓核医学検査による集積異常の部位, 範囲の評価は臨床上有用です。血流SPECTに比べて, 123I-BMIPP や123I-MIBG シンチグラフィでは心尖部を中心とした集積低下所見は高度にみられます。極座標表示にすると、左前下行枝を責任病変とする急性冠症候群と比較し集積低下の範囲が広く鑑別に有用です(図5)。
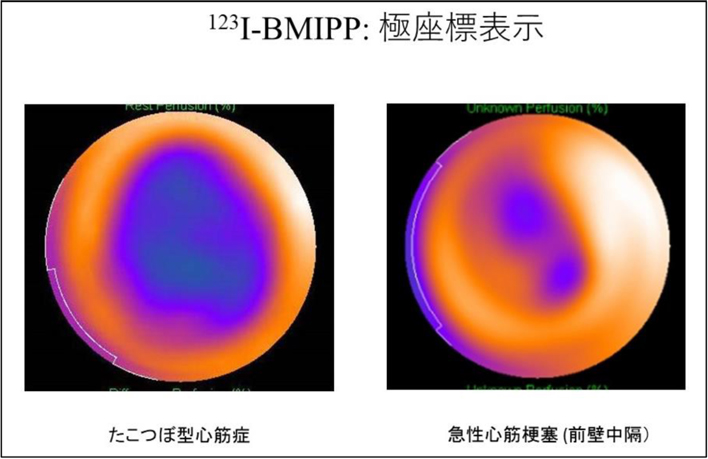
図5. たこつぼ型心筋症と急性前壁心筋梗塞の123I-BMIPPシンチグラフィ極座標表示
心不全の重症度と予後評価: 123I-MIBGを用いた心臓交感神経イメージングは心不全の重症度と予後評価や心不全の治療効果の評価の有用性が認められています。 123I-MIBGの臨床的な評価法として後期像の心/上縦隔比 (heart/mediastinum ratio: H/M比) が臨床的に広く用いられている有用な指標です(図6)。心不全を対象にした123I-MIBGの予後調査研究では, H/M=1.6あるいは1.7以下では致死的イベントを発生する頻度が高く、高リスクとみなされています。
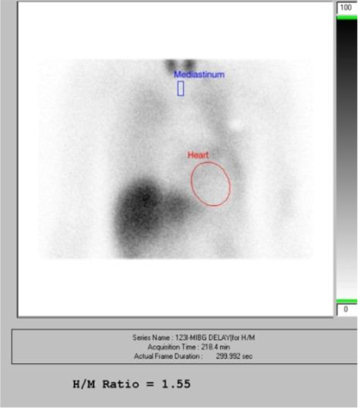
図6. 123I-MIBGの後期像の心/上縦隔比 (heart/mediastinum ratio: H/M比)
心臓CT分野
1)虚血性心疾患
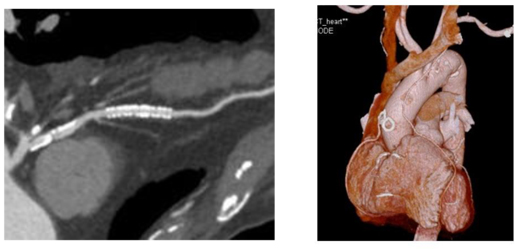
狭心症や心筋梗塞の原因となる冠動脈の狭窄や走行を簡便に評価することが可能です。また、器質的な狭窄の評価だけでなく、プラークの性状や冠動脈の走行異常などの検出にも効果的です。下記は、脂質性プラークに伴う狭窄病変が見られた症例です。CT施行後に緊急カテーテル検査を施行し、ステント治療が行われました。
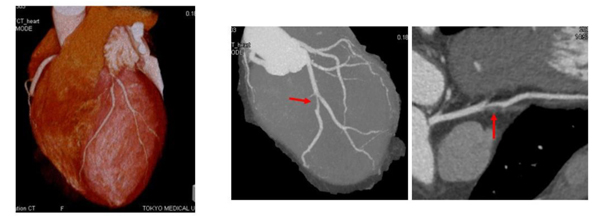
また、ステント治療や冠動脈バイパス術を受けた症例のフォローアップにも冠動脈CTは有用です。
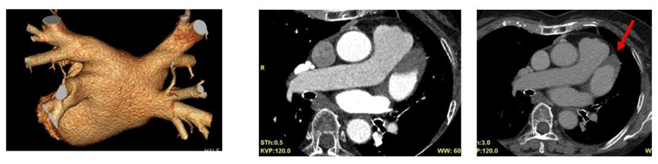
2)左房・肺静脈の形態
近年、心房細動治療に対して、肺静脈隔離術(カテーテルアブレーション)が行われています。アブレーション術前に、肺静脈の解剖学的形態や左房内血栓の有無の評価を行い、アブレーション治療に役立てています。また、術後の肺静脈の形態評価にも有用です。
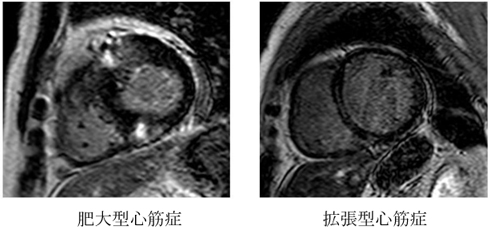
心臓MRI分野
CTとは異なり被ばくの心配がなく、心機能や形態評価を同時に行うことが可能です。造影剤を用いた遅延造影検査では、虚血性心疾患における心筋のバイアビリティや様々な心筋症における心筋変性(線維化)の評価に有用です。
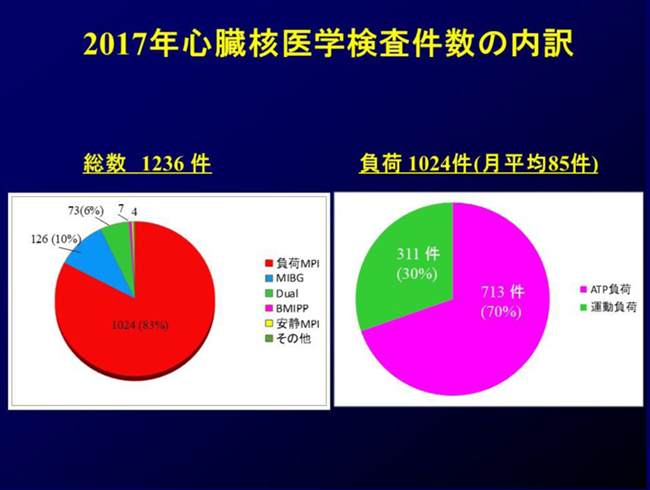
2017年診療実績
心臓核医学検査総数は1236件で、内訳の大部分は負荷心筋シンチグラフィ1024件(83%)です。負荷方法は高齢化を反映して年々薬剤負荷が増加していますが、70%が薬剤負荷、30%が運動負荷でした。
冠動脈CT検査は258件、心臓MRI検査は167件でした。
【2018年】
| 1. | Hirose K, Chikamori T, Hida S, Tanaka N, Yamashita J, Igarashi Y, Saitoh T, Tanaka H, Yamashina A. Application of pressure-derived myocardial fractional flow reserve in chronic hemodialysis patients. J Cardiol. 2018;71:52-58. |
|---|---|
| 2. | Naya M, Uemura Y, Matsumoto N, Momose M, Kato T, Hida S, Yamauchi T, Nakajima T, Suzuki E, Tamaki N; J-COMPASS Extended Follow-Up Study Group. Long-term events after physician-referred initial tests by myocardial perfusion imaging or computed tomography coronary angiography in patients with suspected coronary artery disease. Coron Artery Dis. 2018;29:539-546. |
| 3. | Tezuka D, Kosuge H, Terashima M, Koyama N, Kishida T, Tada Y, Suzuki JI, Sasano T, Ashikaga T, Hirao K, Isobe M. Myocardial perfusion reserve quantified by cardiac magnetic resonance imaging is associated with late gadolinium enhancement in hypertrophic cardiomyopathy. Heart Vessels. 2018; 33:513-52 |
| 4. | 肥田敏・近森大志郎 心臓リモデリングをどう治すか-拡大心・肥大心へのアプローチ-核医学・PETはどこまで進んだか?Heart View 22:841-847,2018. |
| 5. | 肥田敏・近森大志郎 虚血性心疾患診療の現在と未来 核医学検査はどのような時に行うか. Medical Practice 35(9):1371-1376, 2018 |
【2017年】
| 1. | Chikamori T, Goto K, Hida S, Miyagawa M, Ishimura H, Uchida K, Fukuyama T, Mochizuki T, Yamashina A. Diagnostic performance of a semiconductor gamma-camera system as studied by multicenter registry. J Cardiol. 2017;69:449-455. |
|---|---|
| 2. | Hida S. Clinical Performance of the Discovery NM530c in Japanese Patients. Annals of Nuclear Cardiology 2017; 2,125 -130. |
| 3. | Saitoh T, Chikamori T, Hida S, Tanaka H,Igarashi Y, Shiba C, Hirose K, Hatano T, Yamashina A. Dignostic value of lung thallium-201 uptake in detecting high-risk coronary artery disease using cadmium-zinc-telluride camera system. J.Tokyo Med.Univ 2017; 75:305 -314. |
| 4. | Nakajima K, Kudo T, Nakata T, Kiso K, Kasai T, Taniguchi Y, Matsuo S, Momose M, Nakagawa M, Sarai M, Hida S, Tanaka H, Yokoyama K, Okuda K, Edenbrandt L. Diagnostic accuracy of an artificial neural network compared with statistical quantitation of myocardial perfusion images: a Japanese multicenter study. Eur J Nucl Med Mol Imaging. 2017;44:2280-2289. |
| 5. | 肥田敏, 山科章. 123I-MIBG・PETを用いた心血管系自律神経評価. Cardio-Renal Diabetes 2017年6巻1号・4-7頁. |
| 6. | 肥田敏. 循環器内科医による心筋血流SPECT 画像の読影および心筋viability 評価. 日本心臓核医学会誌 2017年19巻・35頁-36頁. |
【2016年】
| 1. | Chikamori T, Hida S, Tanaka N, Igarashi Y, Yamashita J, Shiba C, Murata N, Hoshino K, Hokama Y, Yamashina A. Diagnostic Performance of a Cadmium-Zinc-Telluride Single-Photon Emission Computed Tomography System With Low-Dose Technetium-99m as Assessed by Fractional Flow Reserve. Circ J. 2016 25;80:1217-24. |
|---|---|
| 2. | 肥田敏, 近森大志郎, 五十嵐祐子他. cardioREPOの臨床評価. 臨床放射線. 2016年61巻・725頁-733頁. |
当グループはこれまでも研究テーマについて、教室の他の研究グループと協力し、多くの研究報告を行ってきました。これからも他の研究グループの医師とも一緒に協力し、患者さんの診療に有用な検査を行い、また循環器画像検査の有用性を報告していきたいと考えています。
さらに、2018年10月より、心臓CT/MRIの専門家である小菅寿徳先生が准教授として赴任されました。若手・中堅医師にとっては心臓核医学だけでなく、CT/MRIも併せて、マルチモダリティの非侵襲的評価法を学べる環境が整っています。また来年2019年7月から新病院が開院し、GE社の半導体PET-CT装置が導入予定です。皆さんと協力して循環器画像(イメージング)グループとして発展させていきたいと思います。
当グループではマルチモダリティの非侵襲的評価法の研修を希望される先生を随時募集しております。少しでも興味をもたれた先生はお気軽にご連絡ください。
【連絡先】 肥田敏(ひだ さとし)E-mail: hida-bin@tokyo-med.ac.jp
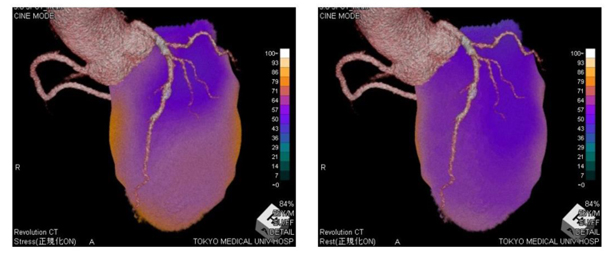
SPECTとCTのfusion画像(左:Stress、右:Rest)
Copyright © Center for Research Administration and Innovation,
Tokyo Medical University. All rights Reserved.